morfologia
No nível macroscópico podemos observar na doença de Alzheimer um grau variável de atrofia (redução da massa de tecidos ou órgãos) cortical, caracterizada pelo aumento dos sulcos parietais, mais acentuado nos lobos frontal, temporal e parietal. Essa atrofia é compensada pelo aumento das cavidades ventriculares secundárias à perda do parênquima (Figura 1). Em particular, nos estágios avançados da doença, as estruturas do lobo temporal medial, incluindo o hipocampo, o córtex entorrinal e a amígdala, são gravemente atrofiadas, dado seu envolvimento a partir dos estágios iniciais da doença.
Além disso, a doença de Alzheimer também apresenta alterações microscópicas, conhecidas como placas senis extracelulares e clusters neurofibrilares intracelulares, que representam a base do diagnóstico histológico. Com a progressão da doença, então, ocorre uma grave perda neuronal acompanhada de gliose (proliferação circunscrita ou difusa, de natureza reativa, de células da neurólise, ou seja, células que constituem o estroma de suporte do tecido nervoso), nas mesmas regiões. onde a presença de placas neurofibrilares e clusters é maior.
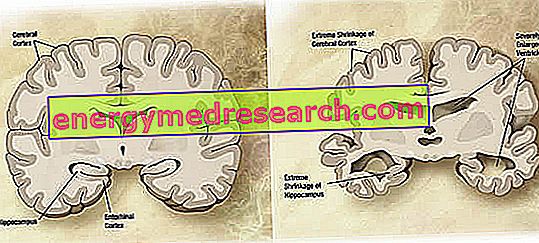
Figura 1. Seção coronal do cérebro: diferenças entre o cérebro normal e o cérebro afetados pela DA (fonte de imagem na Wikipédia).
patogênese
A doença de Alzheimer é caracterizada principalmente por duas lesões típicas: o acúmulo extracelular de placas senis consistindo principalmente do peptídeo β-amilóide (Aβ) e de agregados neurofibrilares intraneuronais, formados pela proteína tau hiperfosforilada.
- As placas senis podem ser encontradas no nível das áreas cerebrais, como hipocampo, amígdala e neocórtex.
O ptido A? Deriva de um corte proteolico do precursor da protea amilde (APP), pela? -Secretase. Este corte gera um fragmento carboxi terminal de 99 resíduos (CTF ou C99) que é subsequentemente cortado por β-secretase para gerar fragmentos Aβ de comprimento diferente. Sabe-se que a espécie mais abundante de Aβ é constituída pelo fragmento Aβ40. Outro fragmento conhecido que se forma a partir do corte proteolítico, menos abundante que Aβ40, é o Aβ42, mais propenso a formar fibrilas amilóides, que se acumulam como espécies Aβ no cérebro de um indivíduo com doença de Alzheimer.
- Outro componente presente na doença de Alzheimer são os aglomerados neurofibrilares que consistem em feixes de filamentos presentes no citoplasma dos neurônios. Os aglomerados neurofibrilares são insolúveis e parecem resistentes aos processos de proteólise in vivo, permanecendo assim presentes nas secções teciduais durante muito tempo após a morte neuronal. Observando a estrutura, as massas fibrilares são constituídas por filamentos de cadeia dupla e filamentos lineares de composição semelhante. Analisando a composição, os filamentos de fita dupla são mais compostos de proteína tau hiperfosforilada. Tau é uma proteína axonal, associada a microtúbulos que facilitam sua montagem.
Outras alterações neuropatológicas importantes na doença de Alzheimer incluem disfunção mitocondrial, dano neuronal oxidativo, perda sináptica e degeneração axonal.
Aspectos Neuroquímicos
Como já explicado, o peptídeo Aβ, derivado do corte proteolítico do precursor de APP, representa um componente neurotóxico da doença de Alzheimer . Especificamente, tem sido hipotetizado que Aβ pode ser importante para funções cerebrais normais e, se exceder algumas concentrações, pode se tornar neurotóxico. Além disso, tanto os agregados quanto as diferentes isoformas de Aβ podem ter um papel biológico, fisiológico ou patológico diferente, determinando e participando dos últimos estágios da doença. De fato, foi observado que o Aβ atua como um neuromodulador, afetando a liberação de alguns neurotransmissores na ausência de sinais evidentes de neurotoxicidade.
Por exemplo, o papel neuromodulador do Aβ, em um contexto fisiológico, poderia ter um significado importante para o equilíbrio correto do sistema neurotransmissor. De fato, sabe-se que esse sistema consiste de neurotransmissores, substâncias que transmitem informações entre as células que compõem o sistema nervoso, os neurônios, através da transmissão sináptica.
Em condições patológicas, em vez disso, a transmissão sináptica mediada por Aβ poderia estar relacionada à alteração da neurotransmissão antes de eventos neurodegenerativos. Como resultado dessas mudanças, podem surgir distúrbios cognitivos e não cognitivos precoces, dependendo dos sistemas de neurotransmissores afetados e das diferentes áreas cerebrais envolvidas.
As alterações dos sistemas neurotransmissores e do mecanismo de transdução de sinal no cérebro de indivíduos afetados pela doença de Alzheimer são muito complexas. Um dos sistemas que é alterado diz respeito ao sistema de sinalização colinérgica, que envolve o neurotransmissor acetilcolina. De fato, tem sido demonstrado que indivíduos afetados pela doença de Alzheimer apresentam uma transmissão colinérgica reduzida ao nível do córtex e do hipocampo, áreas importantes do cérebro responsáveis por fenômenos como aprendizado e memória. Além deste sistema neurotransmissor, também foram observadas alterações na doença de Alzheimer no nível do sistema serotoninérgico noradrenérgico, bem como glutamato e GABA.